Предсказание температуры плавления (критерий Линдемана)
Попытка предсказать точку плавления кристаллических материалов была предпринята в 1910 году Фредериком Линдеманом (англ.). Идея заключалась в наблюдении того, что средняя амплитуда тепловых колебаний увеличивается с увеличением температуры. Плавление начинается тогда, когда амплитуда колебаний становится достаточно большой для того, чтобы соседние атомы начали частично занимать одно и то же пространство.
Критерий Линдемана
утверждает, что плавление ожидается, когда среднеквадратическое значение амплитуды колебаний превышает пороговую величину.
Температура плавления кристаллов достаточно хорошо описывается формулой Линдемана:
T λ = x m 2 9 ℏ 2 M k B θ r s 2 {\displaystyle T_{\lambda }={\frac {x_{m}^{2}}{9\hbar ^{2}}}Mk_{B}\theta r_{s}^{2}}
где r s {\displaystyle r_{s}} — средний радиус элементарной ячейки, θ {\displaystyle \theta } — температура Дебая, а параметр x m {\displaystyle x_{m}} для большинства материалов меняется в интервале 0,15-0,3.
Температура плавления – Расчет
Формула Линдемана выполняла функцию теоретического обоснования плавления в течение почти ста лет, но развития не имела из-за низкой точности.
В 1999г. И.В. Гаврилиным было получено новое выражение для расчёта температуры плавления:
Тпл = DHпл / 1,5 N0 k
, (1)
где Тпл
– температура плавления;DHпл – скрытая теплота плавления;N0 – скрытая теплота плавления;k – константа Больцмана.
Впервые получено исключительно компактное выражение (1) для расчёта температуры плавления металлов, связывающее эту температуру с известными физическими константами: скрытой теплотой плавления, числом Авогадро и константой Больцмана.
Точность расчетов по (1) можно оценить по данным таблицы.
Таблица.
Температура плавления некоторых металлов. Расчет по (1)
| Me | Al | V | Mn | Fe | Ni | Cu | Zn | Sn | Mo |
| DHпл ккал
моль-1 |
2,5 | 5,51 | 3,5 | 4,4 | 4,18 | 3,12 | 1,7 | 1,7 | 8,7 |
| Тпл, К по (1) | 876 | 1857 | 1179 | 1428 | 1406 | 1051 | 583 | 529 | 2945 |
| Тпл, К Эксп. | 933 | 2190 | 1517 | 1811 | 1728 | 1357 | 692 | 505 | 2890 |
По этим данным, точность расчетов Тпл меняется от 2 до 30%, что в расчетах такого рода вполне приемлемо.
Формула (1) выведена как одно из следствий новой теории плавления и кристаллизации, опубликованной в 2000г..
— Гаврилин И.В. Плавление и кристаллизация металлов и сплавов. Изд. ВлГУ. Владимир. 2000. 256 с.
Кинетическая и потенциальная энергия
Чтобы понять, что такое плавление в физике, необходимо ясно представлять соотношение кинетической и потенциальной энергии в твердых и жидких телах.
Потенциальная энергия характеризует работу, которую нужно затратить, чтобы распылить данное тело в пространстве на составляющие его частицы. Для описания этой величины вводят понятие энергии связи, которая обозначает работу, необходимую для того, чтобы оторвать от тела один атом или молекулу и удалить его/ее на бесконечность. Например, типичные значения энергии связи для твердых тел составляют несколько электрон-вольт, эти же значения для жидкостей на порядок меньше.
Кинетическая энергия характеризует интенсивность движения атомов и молекул. В случае конденсированных сред эта энергия прямо пропорционально зависит от температуры.
В твердых телах кинетическая энергия при комнатных температурах составляет несколько сотых электрон-вольт, то есть она в 100 раз меньше потенциальной. Атомы и молекулы в твердых телах находятся как бы в потенциальной яме и колеблются около устойчивых определенных положений. Выбраться они могут из этих положений, если флуктуации кинетической энергии окажутся значительными, или если сама потенциальная яма невелика, например, когда поблизости имеется какой-либо дефект.
Кинетическая энергия атомов и молекул в жидкости приблизительно равна их потенциальной энергии, то есть составляет несколько десятых электрон-вольт при комнатной температуре. Это означает, что каждая частица, составляющая жидкость, постоянно перепрыгивает из одного места в другое. Хорошим доказательством этого факта является Броуновское движение.
https://youtube.com/watch?v=6-SNzUUCYOw
https://youtube.com/watch?v=IC6DTr42oqw
Строение электрических печей для плавки металла
Электродуговая плавка металла производится в электропечи вместимостью от 0,5 до 200 т. Разрабатываются печи на 300 и 400 т. Принципиальная схема устройства дуговой электрической печи показана на рис. 1.
Корпус печи имеет форму цилиндра со сферическим или плоским днищем. Внешне он имеет защитный кожух из стального листа толщиной 10…40 мм, внутренняя поверхность футерована основными или кислыми огнеупорами. Угольные или графитовые электроды пропускаются через отверстия в своде печи. В стенке корпуса имеется рабочее окно, через которое сливают шлак, загружают ферросплавы, отбирают пробы металла.
![]()
Применяют два типа сталеплавильных электропечей: дуговые, и индукционные высокой частоты. Дуговые печи, в которых шихтовые материалы расплавляются теплом электрической дуги, наиболее распространенные благодаря высокому коэффициенту полезного действия, возможности выплавлять в них стали различных марок, простоте строения и удобства обслуживания.
Футеруют печи основными или кислыми огнеупорными материалами. Более распространены печи с основной футеровкой, так как в них можно удалять из жидких сталей серу и фосфор. Современные электродуговые печи оборудованы специальными устройствами, чтобы подводить кислород, используемый для окисления примесей во время плавления стали.
Технология плавки стали в основной дуговой электропечи
В зависимости от состава шихты в электрических печах с основной футеровкой можно плавить сталь тремя методами:
- с полным окислением примесей,
- с частичным их окислением,
- без окисления.
Примечания
- С. Т. Жуков Химия 8-9 класс, Глава 1. Основные представления и понятия химии
- Разброс экспериментальных данных связан, по видимому, с фазовым переходом графит-карбин и различной скоростью нагрева при измерениях. Климовский И. И., Марковец В. В. Влияние фазового перехода графит-карбин на излучательную способность графитовых образцов при их нагревании до температур 3000 K и более // International Scientific Journal for Alternative Energy and Ecology. — 2007. — № 6 (50). — С. 50-59.
- Андреев В. Д. Избранные проблемы теоретической физики.. — Киев: Аванпост-Прим,. — 2012.
- Мейер К. Физико-химическая кристаллография, М., «Металлография», 1972
- Lindemann F. A. // Phys.Z., 1910, v.11, p.609
- Wood W. W., Jacobson J. D. Preliminary Results from a Recalculation of the Monte Carlo Equation of State of Hard Spheres // J. Chem. Phys.. — 1957. — № 27. — С. 1207. — DOI:10.1063/1.1743956.
- Alder B. J., Wainwright T. E. Phase Transition in Elastic Disks // Phys. Rev.. — 1962. — № 127. — С. 359. — DOI:10.1103/PhysRev.127.359.
- Hoover W. G., Gray S. G., Johnson K. W. Thermodynamic Properties of the Fluid and Solid Phases for Inverse Power Potentials // J. Chem. Phys.. — 1971. — № 55. — С. 1128. — DOI:10.1063/1.1676196.
- Пайнс Д. Элементарные возбуждения в твёрдых телах. М., Мир, 1965.
- Андреев В. Д. Крэш (crash)-конформационная кинематика ковалентной решетки алмаза при плавлении. // Журнал структурной химии. — 2001. — № 3. — С. 486-495.
- Андреев В. Д. «Фактор плавления» при межатомных взаимодействиях в алмазной решетке. // Химическая физика. — 2002. — № 8,т.21. — С. 35-40.
Классификация основных видов сварки плавлением
В зависимости от способа передачи тепла методы делятся на газовые и электрические. Последняя технология, в свою очередь, имеет несколько разновидностей.
Рекомендуем к прочтению Как варить металлы в газозащитной среде
Плазменная
Для нагрева используется укороченная дуга. Носителем энергии является электрический разряд. Металл разогревается благодаря воздействию ионизирующего газа. Для запуска процесса требуется повышение температуры до +5500 °С. Принцип действия метода основан на расплавлении материала потоком плазмы, вырабатываемой плазмотроном. Дуга окружена газом, который быстро ионизируется. Заряженные частицы формируют направленный поток. Метод применяют для сварки заготовок из:
- вольфрама;
- молибдена;
- никелевых сплавов;
- нержавеющих сталей.
Плазменная сварка может использоваться для соединения и резки металлических листов толщиной до 1 см.
![]()
Плазменная сварка.
Газовая
Сварка с плавным нагревом используется для скрепления медных, алюминиевых, чугунных, стальных заготовок. Расстояние между соединяемыми деталями заполняют присадочным материалом, который плавится вместе с краями элементов конструкции. Стык прогревают горелкой, пламя в которой образуется при поджигании смеси кислорода и другого газа:
- водорода;
- пропана;
- бутана;
- ацетилена;
- бензиновых или керосиновых паров.
![]()
Газовая сварка. При газовой сварке не используется электрическая энергия, поэтому работы можно выполнять в любых условиях. Недостатком считается невозможность скрепления толстых деталей.
Дуговая
Нагрев металла осуществляется за счет дуги, возникающей при прохождении тока через детали и электрод. Из расплавленных краев заготовок и присадочного материала формируется сварочная ванна. После остывания жидкого металла образуется сварной шов. Способы дуговой сварки классифицируют по таким характеристикам:
- вид электрода (неплавящийся, плавящийся);
- тип тока (постоянный, переменный, с прямой или обратной полярностью);
- уровень механизации (автоматическая, ручная, полуавтоматическая);
- вид дуги (прямая или косвенная);
- способ защиты рабочей зоны (флюсы, использование покрытых электродов или инертного газа).
Присадочный материал должен быть выполнен из того же металла, что и заготовка. При невозможности определения марки стали приобретают переходные электроды. Их же используют для сварки деталей из разнородных сталей. В качестве неплавящихся электродов применяют угольные, вольфрамовые или графитовые стержни.
Рекомендуем к прочтению Все о конденсаторной сварке
![]()
Дуговая сварка.
Лазерная
Разогрев кромок происходит под воздействием луча. Лазерная сварка считается самым точным методом формирования сложных конструкций.
Лазерная сварка подходит для работы с драгоценными и цветными металлами, нержавеющей сталью, титаном. К преимуществам метода относятся:
- отсутствие нагрева прилежащих к шву областей, минимизирующее вероятность деформации;
- возможность работы в труднодоступных местах;
- перевод аппарата в режим резки без использования дополнительных модулей;
- возможность работы без газовой среды и флюса.
![]()
Лазерная сварка. Недостатками считают низкий КПД, высокую стоимость оборудования.
Электрошлаковая
Для плавления металла используется энергия, выделяемая при прохождении тока через слой жидкого шлака. Заготовки устанавливают вертикально, с небольшим расстоянием.
Сварочная ванна поддерживается ползунами. Они перемещаются по мере формирования шва. Электрошлаковая технология применяется для соединения габаритных элементов из никелевых, медных и титановых сплавов. Преимуществом считается формирование шва любой толщины за 1 проход.
![]()
Электрошлаковая сварка.
Индукционная
Заготовка нагревается под воздействием электромагнитной индукции. Для этого применяют высокочастотные токи, проникающие в металл. Шов формируется за несколько секунд. Длительность нагрева не зависит от толщины заготовок или теплопроводности материала. Такая сварка чаще всего применяется для соединения элементов стальных трубопроводов.
Индукционная сварка.
Электронно-лучевая сварка
Источником высокой температуры становится сфокусированный луч, вырабатываемый специальной пушкой. Процесс ведется в вакуумной камере. Плавлению способствует интенсивная бомбардировка металла движущимися с высокой скоростью электронами. Кинетическая энергия частиц при ударах преобразуется в тепловую. Металл расплавляется, образуется шов. Метод распространен в приборостроении, авиации, космической отрасли.
![]()
Электронно-лучевая сварка.
Дуговая
Электродуговая сварка – распространенный вид. Применяется в быту, мелкомасштабном производстве, промышленности. Ее действие основано на получении тепла с помощью дугового разряда, который возникает между электродом и свариваемым металлом. Источник энергии – постоянный или переменный ток.
Под воздействием тепла торец электрода и кромки соединяемых деталей расплавляются, образуется сварочная ванна, некоторое время находящаяся в расплавленном состоянии. Сварное соединение образуется после затвердевания металла.
Виды дуговой сварки зависят от факторов:
- типа дуги – прямого действия (зависимая) или косвенного действия (независимая);
- степени механизации процесса – ручная, полуавтоматическая, автоматическая;
- вида тока и полярности – постоянный ток прямой (на электроде – минус) или обратной (на электроде – плюс) полярности или переменный ток;
- степени защиты участка проводимых работ от атмосферного воздействия – без защиты (голый или со стабилизирующим покрытием электрод), с защитой (шлаковой, шлакогазовой, газовой, комбинированной);
- свойств электрода – сварка плавящимся или неплавящимся электродом.
Плавящимся электродом
Является разновидностью дуговой сварки, при которой электрод расплавляется и служит присадочным материалом. Образование сварного шва происходит в результате расплавления электрода и кромок металла.
Плавящиеся электроды бывают медными, стальными, алюминиевыми.
Неплавящимся электродом
Это процесс, выполняемый с использованием не расплавляющегося во время сварки электрода. Заполнение шва происходит металлом свариваемых деталей. Неплавящиеся электроды представляют собой стержни из электропроводящего материала (угольный, вольфрамовый или графитовый).
![]()
Примерная стоимость вольфрамовых электродов на Яндекс.маркет
Действие требует введения в сварочную ванну присадочной проволоки. При работе с химически активными металлами используют сварку в защитных газах (аргон, гелий, их смесь). Способ находит применение в нефтеперерабатывающей, химической, пищевой, теплоэнергетической, автомобилестроительной сферах. Подходит для соединения цветных металлов и наплавки твердых сплавов.
При какой температуре плавится
Металлические элементы, какими бы они ни были — плавятся почти один в один. Этот процесс происходит при нагреве. Оно может быть, как внешнее, так и внутреннее. Первое проходит в печи, а для второго используют резистивный нагрев, пропуская электричество либо индукционный нагрев. Воздействие выходит практически схожее. При нагреве, увеличивается амплитуда колебаний молекул. Образуются структурные дефекты решётки, которые сопровождаются обрывом межатомных связей. Под процессом разрушения решётки и скоплением подобных дефектов и подразумевается плавление.
У разных веществ разные температуры плавления. Теоретически, металлы делят на:
- Легкоплавкие – достаточно температуры до 600 градусов Цельсия, для получения жидкого вещества.
- Среднеплавкие – необходима температура от 600 до 1600 ⁰С.
- Тугоплавкие – это металлы, для плавления которых требуется температура выше 1600 ⁰С.
Плавление железа
Температура плавления железа достаточно высока. Для технически чистого элемента требуется температура +1539 °C. В этом веществе имеется примесь — сера, а извлечь ее допустимо лишь в жидком виде.
Интересное: Как варить чугун
Без примесей чистый материал можно получить при электролизе солей металла.
Плавление чугуна
Чугун – это лучший металл для плавки. Высокий показатель жидкотекучести и низкий показатель усадки дают возможность эффективнее пользоваться им при литье. Далее рассмотрим показатели температуры кипения чугуна в градусах Цельсия:
- Серый — температурный режим может достигать отметки 1260 градусов. При заливке в формы температура может подниматься до 1400.
- Белый — температура достигает отметки 1350 градусов. В формы заливается при показателе 1450.
Важно! Показатели плавления такого металла, как чугун – на 400 градусов ниже, по сравнению со сталью. Это значительно снижает затраты энергии при обработке
Плавление стали
![]()
Плавления стали при температуре 1400 °C Сталь — это сплав железа с примесью углерода. Её главная польза — прочность, поскольку это вещество способно на протяжении длительного времени сохранять свой объем и форму. Связано это с тем, что частицы находятся в положении равновесия. Таким образом силы притяжения и отталкивания между частицами равны.
Справка! Сталь плавится при 1400 °C.
Плавление алюминия и меди
Температура плавления алюминия равна 660 градусам, это означает то, что расплавить его можно в домашних условиях.
Чистой меди – 1083 градусов, а для медных сплавов составляет от 930 до 1140 градусов.
1.3. Гомогенная (самопроизвольная) кристаллизация [3].
Самопроизвольная кристаллизация обусловлена стремлением вещества иметь более устойчивое состояние, характеризуемое уменьшение термодинамического потенциалы G. С повышением температуры термодинамический потенциал вещества как в твердом, так и в жидком состоянии уменьшается. Температура, при которой термодинамические потенциалы в твердом и жидком состоянии равны, называется равновесной температурой кристаллизации. Кристаллизация происходит в том случае, если термодинамический потенциал в твердом состоянии будет меньше термодинамического потенциала в жидком состоянии, т. е. при переохлаждении жидкого металла до температр ниже равновесной. Зарождение кристаллов может быть определено как процесс образования в какой-либо ограниченной части объема новой фазы, отделенной от остального вещества границей раздела. В случае затвердевания зарождение заключается в образовании в жидкости мельчайших частиц твердой фазы (центров кристаллизации).
Для ответа на вопрос о том, как и когда произошло зарождение центров кристаллизации, необходимо рассмотреть проблему зарождения как с термодинамической, так и с кинетической точки зрения. С термодинамической точки зрения существует только одна температура, при которой чистый металл в твердом состоянии может находиться в равновесии с чистым жидким металлом. При этой температуре свободные энергии двух фаз равны. Ниже температуры кристаллизации или плавления твердая фаза является стабильной, так как она обладает меньшей свободной энергией; выше температуры кристаллизации — стабильна жидкая фаза. Ниже точки плавления металл должен находиться в твердом состоянии, так как в этом случае переходу из жидкого состояния в твердое соответствует уменьшение объемной свободной энергии системы. То есть чем больше величина переохлаждения, тем больше выигрыш в свободной энергии, получаемый при переходе из жидкого состояния в твердое. Если изменение свободной энергии отрицательно при превращении переохлажденной жидкости в твердое тело, то почему это превращение не происходит сразу же после того, как температура расплава окажется ниже равновесной температуры кристаллизации? Выше рассматривалось лишь изменение объемной свободной энергии системы. Когда же атомы группируются таким образом, что образуется зародыш или центр кристаллизации, то между ним и жидкостью возникает поверхность раздела. Образование поверхности раздела приводит к затрате энергии, что вызывает некоторое увеличение свободной энергии системы при возникновении зародыша. Зародыш может расти только в том случае, если суммарная свободная энергия системы уменьшается.
4 стр., 1875 слов
Агрегатное состояние вещества
… рассмотреть следующие агрегатные сотояния: 1. газ 2. жидкости 3. твердые вещества 4. плазма 1. Агрегатное состояние вещества — газ Газы (французское gaz; название предложено голланским … твёрдое состояние — кристаллизацией или (в зависимости от величины приложенного давления) фазовым переходом в сверхтекучее состояние для 4He и в жидко-анизотропное состояние для жидких кристаллов. При давлениях ниже …
Плавление и кристаллизация
![]()
Подробности Категория: Молекулярно-кинетическая теория 06.11.
2014 13:52 10986
Одно и то же вещество при определённых условиях может находиться в различных агрегатных состояниях — твёрдом, жидком или газообразном.
При переходе из одного состояния в другое состав молекул этого вещества не меняется. Изменяется только их расположение, характер теплового движения и силы межмолекулярного воздействия.
Из твёрдого состояния вещество переходит в жидкое, а из жидкого в газообразное. Такой переход называют фазовым переходом.
Плавление
При низких температурах все вещества замерзают и превращаются в твёрдые тела, атомы и молекулы в которых упакованы так плотно, что силы их взаимного притяжения позволяют им совершать только колебательные движения около положения равновесия. Поэтому при обычных условиях твёрдые тела сохраняют объём и форму.
Процесс перехода вещества из твёрдого состояния в жидкое называют плавлением. Это процесс происходит при повышении температуры.
Весной, когда пригревает солнышко, начинают таять снежные сугробы. Мельчайшие кристаллики льда, из которых состоит снег, превращаются в воду.
Но, несмотря на то, что воздух прогревается, и его температура становится выше нуля, температура тающего снега, и температура талой воды остаются равными 00С до тех пор, пока снег не растает совсем. Всё дело в том, что плавление происходит постепенно.
Вещество при плавлении поглощает тепло, которое получает извне, и некоторое время одновременно находится и в твёрдом, и в жидком состоянии. И его температура не меняется, пока всё оно не расплавится и не станет жидким.
Что происходит при нагревании твёрдого вещества? При повышении температуры скорость колебаний частиц внутри вещества увеличивается. Следовательно, увеличивается и его внутренняя энергия.
При определённой температуре, которую называют температурой плавления, кристаллическая решётка твёрдого тела начинает разрушаться. Молекулы получают большую свободу.
Чтобы твёрдое вещество начало плавиться, его необходимо нагреть до температуры плавления. Когда оно начинает получать тепло извне, некоторое время его температура будет расти прямо пропорционально времени нагревания.
Так будет до тех пор, пока оно не начнёт плавиться. Но как только его температура станет равной температуре плавления, она перестанет изменяться и будет постоянной, пока всё вещество не превратится в жидкость.
После этого температура жидкости снова начнёт повышаться.
Но если жидкость перестанет получать тепло, она начнёт остывать. И как только её температура снизится до значения, равного температуре плавления, начинается процесс кристаллизации.
Каждое вещество имеет свою температуру плавления. При нормальном давлении (760 мм рт.ст.) лёд начинает плавиться при 0оС. Самую высокую температуру плавления среди металлов имеет вольфрам — 3422 °C. Простое вещество углерод плавится при температуре 3500 — 4500 °C. А температура плавления спирта — минус 114оС.
Ионная кристаллическая решетка
![]()
В случае, если в узлах кристалла находятся заряженные частицы – ионы, мы можем говорить о ионной кристаллической решетке. Как правило, с ионных кристаллах чередуются положительные ионы (катионы) и отрицательные ионы (анионы), поэтому частицы в кристалле удерживаются силами электростатического притяжения. В зависимости от типа кристалла и типа ионов, образующих кристалл, такие вещества могут быть довольно прочными и тугоплавкими. В твердом состоянии подвижных заряженных частиц в ионных кристаллах, как правило, нет. Зато при растворении или расплавлении кристалла ионы высвобождаются и могут двигаться под действием внешнего электрического поля. Т.е. проводят ток только растворы или расплавы ионных кристаллов. Ионная кристаллическая решетка характерна для веществ с ионной химической связью. Примеры таких веществ – поваренная соль NaCl, карбонат кальция – CaCO3 и др. Ионную кристаллическую решетку, как правило, в твердой фазе образуют соли, основания, а также оксиды металлов и бинарные соединения металлов и неметаллов.
![]()
Связь между частицами в ионных кристаллах: ионная химическая связь.
В узлах кристалла с ионной решеткой расположены ионы.
Фазовое состояние ионных кристаллов при нормальных условиях: как правило, твердые вещества.
Химические вещества с ионной кристаллической решеткой:
- Соли (органические и неорганические), в том числе соли аммония (например, хлорид аммония NH4Cl);
- Основания;
- Оксиды металлов;
- Бинарные соединения, в составе которых есть металлы и неметаллы.
Физические свойства веществ с ионной кристаллической структурой:
— высокая температура плавления (тугоплавкость);
— растворы и расплавы ионных кристаллов – проводники тока;
— большинство соединений растворимы в полярных растворителях (вода);
— твердое фазовое состояние у большинства соединений при нормальных условиях.
Физика 8 класс. Плавление и кристаллизация
Физика 8 класс Конспект Плавление
![]()
Плавление и кристаллизация. Удельная теплота плавления.
Задачи на тему Тепловые явления
Переход вещества из твердого состояния в жидкое называется плавлением.
Плавление кристаллических тел происходит только при определенной температуре.
Температуру, при которой вещество плавится, называют температурой плавления вещества.
Чтобы провести процесс плавления, сначала надо нагреть твердое тело до температуры плавления.
Если тело нагреть до температуры плавления и убрать нагреватель (перестать подводить тепло к телу) — то плавления не происходит.
Чтобы осуществить плавление тела, надо выполнить два условия: 1. нагреть тело до температуры плавления 2. продолжить передачу теплоты
Температура плавления — важная тепловая характеристика вещества. У разных веществ температура плавления различна.
![]()
Плавление металла
Переход вещества из жидкого состояния в твердое называют отвердеванием или кристаллизацией.
Чтобы началась кристаллизация расплавленного (жидкого) тела, оно должно остыть до определенной температуры.
Температура, при которой вещество отвердевает (кристаллизуется), называют температурой отвердевания или кристаллизации.
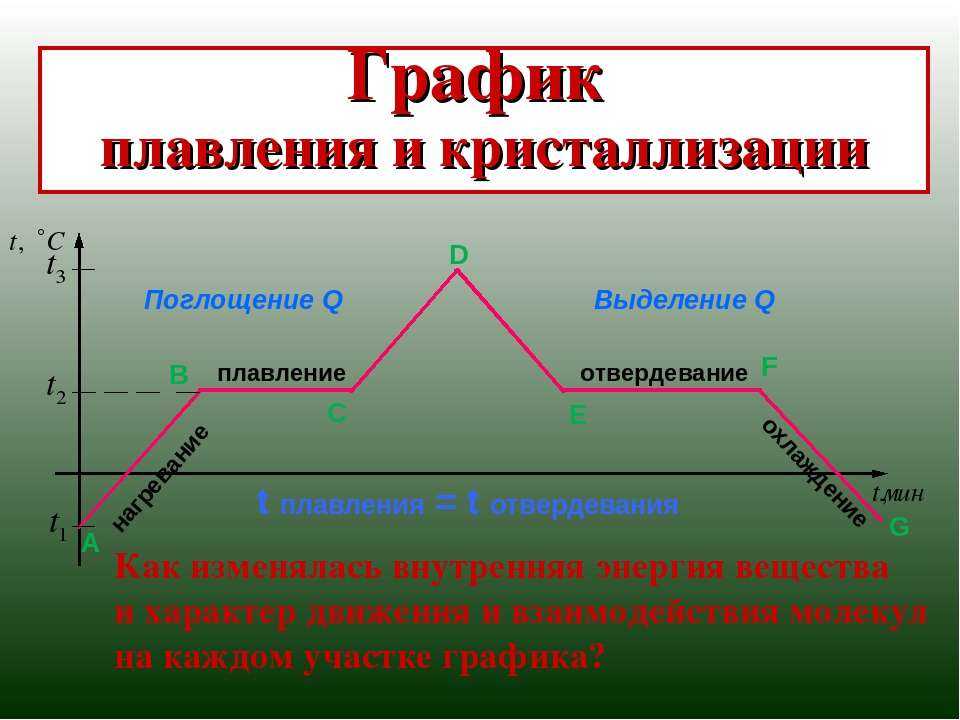
График плавления и отвердевания кристаллических тел.
![]()
График плавления и отвердевания
Опыт показывает, что вещества отвердевают при той же температуре, при которой плавятся.
Чтобы осуществить процесс отвердевания нужно выполнить два условия: 1. охладить жидкость до температуры отвердевания (плавления) 2. продолжать отводить тепло до тех пор, пока вся жидкость не отвердеет.
Физическая величина, показывающая, какое количество теплоты необходимо сообщить кристаллическому телу массой 1 кг, чтобы при температуре плавления полностью перевести его в жидкое состояние, называется удельной теплотой плавления.
Удельную теплоту плавления обозначают буквой λ, измеряют в Дж/кг.
Чтобы вычислить количество теплоты Q, необходимое для плавления кристаллического тела массой m, взятого при его температуре плавления и нормальном атмосферном давлении,
нужно удельную теплоту плавления λ умножить на массу тела:
где Q– количество теплоты, m– масса тела.
Температура плавления и кристаллизации для данного вещества при неизменном внешнем давлении равны.
![]()
Кристаллизация
Количество теплоты, выделяющееся при кристаллизации вещества, при неизменном внешнем давлении равно количеству теплоты, полученному этим веществом при плавлении.
Задачи
Испарение и конденсация
Конспект составлен на основании теоретического материала учебника «Физика 8 класс» А.В. Перышкин, «Физика 8 класс»А.В.Грачев.
Скачать конспект:
teoriya_8_plavleniekristallizacziya
Физика 8 класс. Тепловые явления. Теплопередача.
Физика 8 класс. Количество теплоты. Удельная теплоемкость. Топливо.
Физика 8 класс. Электрический ток. Сила тока
Физика 8 класс. Испарение. Насыщенный пар. Влажность воздуха.
Плавление в домашних условиях
Благодаря низкой температуре плавления древние люди могли расплавлять купрум на костре и использовать металл для изготовления различных изделий.
Для расплавки меди в домашних условиях понадобится:
- древесный уголь;
- тигель и специальные щипцы для него;
- муфельная печь;
- бытовой пылесос;
- горн;
- стальной крюк;
- форма для плавления.
Процесс течет поэтапно, металл помещается в тигель, а затем размещается в муфельной печи. Выставляется нужная температура, а наблюдение за процессом осуществляется через стеклянное оконце. В процессе в емкости с Cu появится окисная пленка, которую нужно устранить — открыть окошко и отодвинуть в сторону стальным крюком.
При отсутствии муфельной печи расплавить медь можно автогеном. Плавление пойдет, если ест нормальный доступ воздуха. Паяльной лампой расплавляется латунь и легкоплавкая бронза. Пламя должно охватить весь тигель.
Если под рукой ничего из перечисленных средств нет, можно использовать горн, установленный на слой древесного угля. Для повышения Т можно использовать пылесос, включенный в режим выдувания, но шланг должен иметь металлический наконечник, хорошо, если с зауженным концом, так струя воздуха будет тоньше.
Температура плавления бронзы и латуни, как температура плавления меди и алюминия — невысоки.
Сегодня в промышленных условиях в чистом виде Cu не используется. В ее составе содержится много примесей: никель, железо, мышьяк, сурьма, другие элементы. Качество продукта определяется наличием содержания в процентах примесей в сплаве (не более 1%). Важные показатели — тепло- и электропроводность. Благодаря пластичности, малой Т плавления и гибкости медь широко используется во многих отраслях промышленности.
Читать также: Обозначение контактора на однолинейной схеме
Другие варианты определений к слову :
2.
Первый металл в таблице Менделеева.
3.
Металл, который мягче воска и легче дерева.
7.
«Литос» по-гречески «камень», а какой металл получил шведский химик Арфедсон самым первым из царства камней?
8.
Батискаф и атомная бомба, пиротехника и лечение психозов – вот области применения этого химического элемента.
9.
Своё название этот химический элемент получил из-за того, что был обнаружен в камнях.
10.
Этот щелочной металл был воспет большим любителем химии Куртом Кобэйном.
Температура плавления
(обычно совпадает с температурой кристаллизации) — температура, при которой твёрдое кристаллическое тело совершает переход в жидкое состояние и наоборот. При температуре плавления вещество может находиться как в жидком, так и в твёрдом состоянии. При подведении дополнительного тепла вещество перейдёт в жидкое состояние, а температура не будет изменяться, пока всё вещество в рассматриваемой системе не расплавится. При отведении лишнего тепла (охлаждении) вещество будет переходить в твёрдое состояние (застывать), и, пока оно не застынет полностью, его температура не изменится.
Температура плавления/отвердевания и температура кипения/конденсации считаются важными физическими свойствами вещества. Температура отвердевания совпадает с температурой плавления только для чистого вещества. На этом свойстве основаны специальные калибраторы термометров для высоких температур. Так как температура застывания чистого вещества, например олова, стабильна, достаточно расплавить и ждать, пока расплав не начнёт кристаллизоваться. В это время, при условии хорошей теплоизоляции, температура застывающего слитка не изменяется и в точности совпадает с эталонной температурой, указанной в справочниках.
Смеси веществ не имеют температуры плавления/отвердевания вовсе и совершают переход в некотором диапазоне температур (температура появления жидкой фазы называется точкой солидуса, температура полного плавления — точкой ликвидуса). Поскольку точно измерить температуру плавления такого рода веществ нельзя, применяют специальные методы (ГОСТ 20287 и ASTM D 97). Но некоторые смеси (эвтектического
состава) обладают определенной температурой плавления, как чистые вещества.
Аморфные (некристаллические) вещества, как правило, не обладают чёткой температурой плавления. С ростом температуры вязкость таких веществ снижается, и материал становится более жидким.
Поскольку при плавлении объём тела изменяется незначительно, давление мало влияет на температуру плавления. Зависимость температуры фазового перехода (в том числе и плавления, и кипения) от давления для однокомпонентной системы даётся уравнением Клапейрона-Клаузиуса. Температуру плавления при нормальном атмосферном давлении (101 325 Па, или 760 мм ртутного столба) называют точкой плавления
Читать также: Рассверливание отверстий в металле